Jede Cannabissorte hat ein einzigartiges Cannabinoid- und Terpenprofil, das ihr einen chemisch individuellen „Fingerabdruck“ verleiht. Dieses Profil bestimmt die medizinisch bedeutsamen Effekte. Aber erst seit der Entdeckung der Cannabinoidrezeptoren und somit des Endocannabinoidsystems in den 1990er Jahren begann man das volle medizinische Potential der Cannabispflanze und das komplexe Zusammenspiel ihrer Wirkstoffe auf wissenschaftlicher Ebene zu verstehen.
Cannabinoide
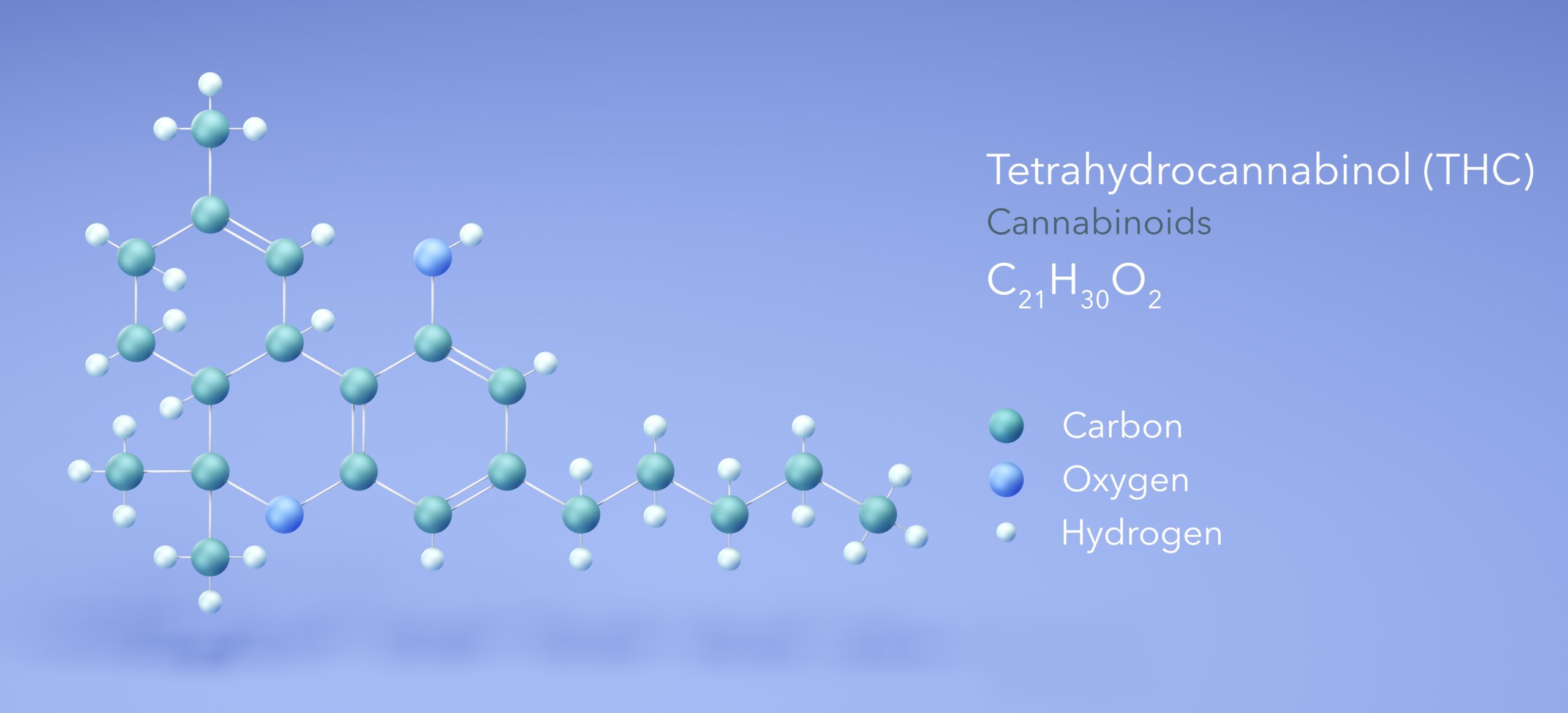
Unser Endocannabinoidsystem kann nicht nur mit unseren körpereigenen Cannabinoiden, den sogenannten Endocannabinoiden, wie beispielsweise Anamdamid interagieren, sondern auch mit den in der Cannabispflanze vorkommenden Phytocannabinoiden. Dazu zählen insbesondere die beiden wichtigsten Cannabinoide: Tetrahydrocannabinol (THC) und Cannabidiol (CBD). Denn diese beiden Cannabinoide liegen in der Pflanze meist in den höchsten Konzentrationen vor. Aber es gibt noch zahlreiche weitere Cannabinoide, von denen einige aktuell an Bedeutung gewinnen. Die Cannabinoide liegen in der Pflanze zumeist als Säuren (z.B. THCA) vor. Um ihre Wirkung jedoch vollständig zu entfalten, müssen sie umgewandelt werden, wie z.B. durch die Hitze beim Verdampfen. Dieser Vorgang wird auch als Decarboxylierung bezeichnet. Durch die unterschiedliche Zusammensetzung und Konzentration der Wirkstoffe in Cannabispflanzen, bietet sich die Möglichkeit einer sehr individuellen Therapie, die auf die Bedürfnisse des oder der jeweiligen Patient:in abgestimmt ist.
Tetrahydrocannabinol (THC)
THC wurde in den 1960er Jahren von Raphael Mechoulam entdeckt und ist das wohl bekannteste und medizinisch meist eingesetzte Cannabinoid der Welt. Seine psychoaktive Wirkung trug dabei maßgeblich zum Verbot von Cannabis bei. Die Bindung von THC an die Cannabinoidrezeptoren moduliert die Signalübertragung und wirkt somit auf das zentrale und periphere Nervensystem. Dieser Mechanismus führt unter anderem zu schmerzlindernden, muskelrelaxierenden, appetitstimulierenden, schlaffördernden oder stimmungsaufhellenden Effekten. THC findet daher vor allem bei der Behandlung von chronischen und neuropathischen Schmerzen, MS-induzierter Spastik, Chemotherapie-induzierter Übelkeit und Erbrechen oder bei Anorexie/Wasting (Auszehrungssyndrom) Anwendung. Darüber hinaus wird es aber auch erfolgreich bei einer Vielzahl weiterer Erkrankungen und Symptome wie z.B. Tic-Störungen, Post-Traumatischer Belastungsstörung, ADHS, Migräne oder im Bereich der Palliativmedizin eingesetzt. Bezogen auf randomisierte und Placebo-kontrollierte klinische Studien, ist THC das wohl am besten untersuchte Cannabinoid. Dennoch bleibt auch THC weiterhin Gegenstand der Forschung, um die genauen Wirkmechanismen und Interaktionen mit anderen Wirkstoffen der Cannabispflanze noch besser zu verstehen.
Cannabidiol (CBD)
Verglichen mit THC weist CBD eine geringe Affinität für die Cannabinoidrezeptoren auf. Allerdings kann es über andere Mechanismen den Abbau der körpereigenen Cannabinoide (Endocannabinoide) hemmen. Zudem bindet CBD an eine ganze Reihe weiterer Rezeptoren, die unter anderem an der Vermittlung entzündungshemmender Prozesse, der Schmerzwahrnehmung, der Reduktion epileptischer Episoden sowie der Regulation von Angst beteiligt sind. Darüber hinaus hat CBD im Gegensatz zu THC keine berauschende Wirkung. Die komplexen Wirkmechanismen von CBD und das damit verbundene breite Einsatzgebiet sind derzeit Gegenstand ausgiebiger Forschung, dennoch ergibt sich aus diesen zahlreichen Interaktionen ein breites Spektrum an potentiellen Einsatzgebieten.
Zu den bekanntesten Anwendungsbereichen von Cannabidiol zählen unter anderem schmerzhafte Erkrankungen mit entzündlichen Komponenten wie beispielsweise chronisch entzündliche Darmerkrankungen oder Rheumatoide Arthritis aber auch Stress, Angststörungen und Psychosen. In Form eines Fertigarzneimittels wird CBD auch sehr erfolgreich bei schweren Epilepsieerkrankungen bei Kindern eingesetzt.
Cannabigerol (CBG)
Cannabigerol ist die Vorstufe zu fast allen anderen Cannabinoiden und kommt normalerweise nur in sehr geringen Mengen in Cannabis vor. Ähnlich wie bei CBD, besitzt auch Cannabigerol keine berauschende Wirkung. Einige Grundlagenstudien deuten darauf hin, dass CBG unter anderem schmerzlindernde, entzündungshemmende, neuroprotektive und blutdrucksenkende Eigenschaften besitzt. Allerdings sind sowohl die Wirkungen als auch mögliche Nebenwirkungen aufgrund fehlender Studien am Menschen nicht ausreichend untersucht.
Cannabinol (CBN)
CBN war das erste Cannabinoid, das bereits 1896 identifiziert und aus Cannabis isoliert wurde. Es entsteht als Oxidationsnebenprodukt von THC, beispielsweise nach längerer Lagerung durch die Einwirkung von Luft, Hitze oder Licht. CBN ist ein viel weniger starkes Cannabinoid als THC, das über eine sehr geringe psychoaktive Wirkung verfügt. Entgegen der weit verbreiteten Meinung konnten bisher nur wenige Wirkungen mit einem direkten medizinischen Nutzen nachgewiesen werden. So zeigten sich beispielsweise eine schwache schmerzlindernde Wirkung bei einem Tiermodell für myofasziale Schmerzen. Schlaffördernde Effekte zeigten sich lediglich beim Einsatz sehr hoher Dosen und ein möglicher Einsatz bei allergischen Atemwegserkrankungen ist noch nicht ausreichend untersucht.
Tetrahydrocannabivarin (THCV)
Tetrahydrocannabivarin (THCV), ein Analogon von THC, das aus Cannabigerovarinsäure (CBGVA) gebildet wird, das neben CBGA einer der beiden wichtigsten Vorläufer von Cannabinoiden ist. Es gibt Hinweise darauf, dass THCV in höheren Dosen ein eher „klares, aktivierendes High“ erzeugt. Dennoch gilt es bisher in klinischen Versuchen als gut verträglich. In verschiedenen Studien zeigten sich schmerzlindernde, appetithemmende, antientzündliche und neuroprotektive Eigenschaften. Aktuell werden aber vor allem die potenziellen antidiabetischen Effekte von THCV und ein möglicher Einsatz bei der Behandlung von Typ-2-Diabetes durch die Regulierung des Blutzuckerspiegels und einer möglichen Verringerung der Insulinresistenz in klinischen Studien untersucht.
Cannabidivarin (CBDV)
Cannabidivarin (CBDV) ist ein Analogon von CBD, das wie CBD keine psychoaktive Wirkung hat. Derzeit gilt Cannabidivarin als eines der vielversprechenderen Cannabinoide, die zur Behandlung schwerer Erkrankungen zum Einsatz kommen könnten. Klinische Forschungsergebnisse lassen darauf schließen, das CBDV vor allem bei Epilepsie und Autismus-Spektrum-Störungen Anwendung finden könnte. Zudem erhielt es 2018 von der Europäischen Arzneimittel-Agentur (EMA) den Orphan-Status für die Behandlung schwerer und seltener Erkrankungen wie das Rett-Syndrom und das Fragile-X-Syndrom.
Flavonoide
Wie in anderen Pflanzen auch sind die Flavonoide in der Cannabispflanze vor allem für die Farbe, aber auch den Geruch und den Geschmack verantwortlich. Flavonoide dienen Pflanzen vor allem als Schutz vor z.B. UV-Strahlung oder der Abwehr von Schädlingen, aber auch zum Anlocken von Insekten für die Bestäubung. Bisher sind rund 8.000 Flavonoide bekannt, die in einzelne Kategorien eingeteilt werden können. Zu den bekanntesten Flavonoiden, die in Cannabispflanzen zu finden sind, zählen unter anderem Apigenin, Cannflavin A, Cannflavin B, Kaempferol oder Vitexin. Man geht davon aus, dass Flavonoide bei zahlreichen Erkrankungen einen positiven Effekt haben können. Ähnlich wie bei Terpenen werden entzündungshemmende, gefäßschützende, durchblutungsfördernde sowie neuroprotektive und antioxidative Wirkungen der Flavonoide vermutet. Doch sind noch längst nicht alle Flavonoide und ihre genauen Wirkungen ausreichend erforscht.
Terpene
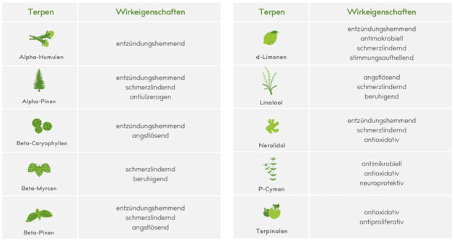
Darüber hinaus enthält die Cannabispflanze bedeutende ätherische Öle – die Terpene. Diese sind zum einen verantwortlich für den Geruch und den Geschmack, entfalten aber auch eigene medizinische Wirkungen. Mittlerweile gewinnen Terpene auch an Bedeutung als Aromastoffe in Produkten wie Vapes, Esswaren, Schönheits -und Hautpflegeprodukten.
Im Vergleich zu anderen Pflanzen ist Cannabis generell reich an Terpenen. So enthält 1 g Cannabis zwischen 5 und 35 mg dieser aromatischen Stoffe. Doch nicht nur wegen des Aromas wählen viele Patienten bestimmte Cannabissorten, sondern auch weil sie sich von der jeweiligen Zusammensetzung der Terpene eine Wirkung auf bestimmte Symptome erwarten.
Aber welchen realen Einfluss haben die Terpene auf die Wirkung von Medizinalcannabis?
Unter Forschern besteht kein Konsens über die Beantwortung dieser Frage. Tatsache ist, dass viele Terpene eine eigene pharmakologische Wirkung besitzen, die in Zell- und Tierstudien nachgewiesen werden konnte. Einige Argumente sprechen jedoch gegen eine vergleichbare Wirkung bei der Einnahme von Medizinalcannabis. Nur ein kleiner Teil der eingenommenen Menge an Terpenen gelangt bei der Einnahme tatsächlich in die Blutbahn. Dazu kommt, dass eine Wirksamkeit erst bei Konzentrationen nachweisbar ist, die bei üblichen Dosierungen nicht erreicht werden können. Zudem fehlen Daten aus Studien am Menschen.
Zusammenfassend kann man sagen, dass auch wenn Terpene definitiv über ein gewisses medizinisches Potenzial verfügen, die häufig berichteten spezifischen Wirkungen in Zusammenhang mit Medizinalcannabis aber oftmals etwas optimistisch sind. Dennoch können die Terpene die Wirkung von Cannabinoiden beeinflussen. Das liegt vermutlich hauptsächlich am sogenannten Entourage-Effekt, bei dem es zu einer passiven Verstärkung oder auch Abschwächung der einzelnen Wirkungen durch die Interaktion mit weiteren Stoffen kommt. Zudem kann die genaue Wirkweise von bestimmten Cannabissorten von Patient:in zu Patient:in sehr unterschiedlich sein.
Quellen:
- Russo, E. B. (2011). Taming THC: potential cannabis synergy and phytocannabinoid‐terpenoid entourage effects. British journal of pharmacology, 163(7), 1344-1364.
- Grotenhermen, F., Müller-Vahl, K. (2016). Medicinal uses of marijuana and cannabinoids. Critical Reviews in Plant Sciences, 35(5-6), 378-405.
- Pisanti, S., Malfitano, A. M., Ciaglia, E., Lamberti, A., Ranieri, R., Cuomo, G., Laezza, C. (2017). Cannabidiol: State of the art and new challenges for therapeutic applications. Pharmacology & therapeutics, 175, 133-150.
- De Meijer, E. P. M., Hammond, K. M., & Micheler, M. (2009). The inheritance of chemical phenotype in Cannabis sativa L. (III): variation in cannabichromene proportion. Euphytica, 165(2), 293-311.
- Russo, E. B., & Marcu, J. (2017). Cannabis pharmacology: the usual suspects and a few promising leads. Advances in pharmacology, 80, 67-134.
- Walsh, K. B., McKinney, A. E., & Holmes, A. E. (2021). Minor Cannabinoids: Biosynthesis, Molecular Pharmacology and Potential Therapeutic Uses. Frontiers in pharmacology, 12.
- Wong, H., & Cairns, B. E. (2019). Cannabidiol, cannabinol and their combinations act as peripheral analgesics in a rat model of myofascial pain. Archives of oral biology, 104, 33-39.
- Jadoon, K. A., Ratcliffe, S. H., Barrett, D. A., Thomas, E. L., Stott, C., Bell, J. D., … & Tan, G. D. (2016). Cannabidiol (CBD) and D9-tetrahydrocannabivarin (THCV) are nonpsychoactive phytocannabinoids affecting lipid and glucose metabolism in animal models. This study set out to examine the effects of these compounds in patients with type 2 diabetes. Diabetes Care, 39, 1-10.
- Wargent, E. T., Zaibi, M. S., Silvestri, C., Hislop, D. C., Stocker, C. J., Stott, C. G., … & Cawthorne, M. A. (2013). The cannabinoid Δ9-tetrahydrocannabivarin (THCV) ameliorates insulin sensitivity in two mouse models of obesity. Nutrition & diabetes, 3(5), e68-e68.
- Morano, A., Cifelli, P., Nencini, P., Antonilli, L., Fattouch, J., Ruffolo, G., … & Giallonardo, A. T. (2016). Cannabis in epilepsy: From clinical practice to basic research focusing on the possible role of cannabidivarin. Epilepsia open, 1(3-4), 145-151. doi: 10.1002/epi4.12015
- Zamberletti, E., Rubino, T., & Parolaro, D. (2021). Therapeutic potential of cannabidivarin for epilepsy and autism spectrum disorder. Pharmacology & Therapeutics, 226, 107878. DOI: 10.1016/j.pharmthera.2021.107878
- Baron, E. P. (2018). Medicinal Properties of Cannabinoids, Terpenes, and Flavonoids in Cannabis, and Benefits in Migraine, Headache, and Pain: An Update on Current Evidence and Cannabis Science. Headache: The Journal of Head and Face Pain, 58(7), 1139–1186. doi:10.1111/head.13345